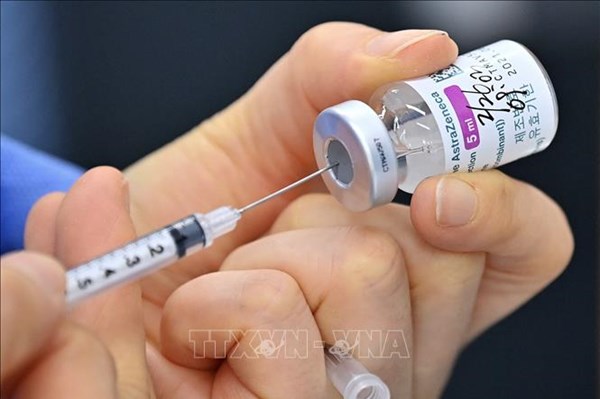
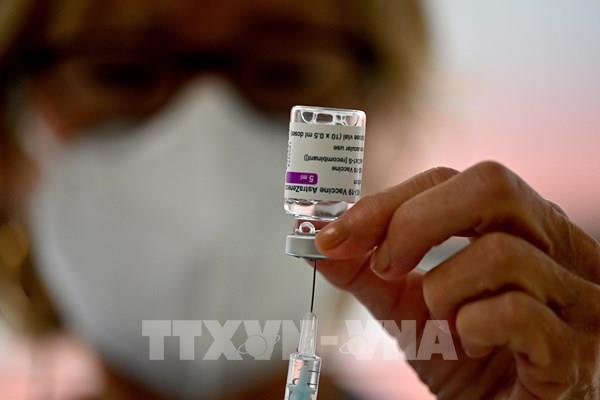
FDA cấp phép cho cocktail kháng thể phòng COVID-19 của Astrazeneca
Cơ quan Quản lý Thực phẩm và Dược phẩm của Mỹ (FDA) ngày 8/12 đã cấp phép sử dụng liệu pháp hỗn hợp kháng thể Evusheld (cocktail kháng thể) của hãng AstraZeneca để ngăn ngừa COVID-19 ở những người có hệ thống miễn dịch kém hoặc có tiền sử bị tác dụng phụ với các vaccine phòng bệnh này.
FDA nên rõ cocktail kháng thể Evusheld chỉ được cấp phép sử dụng cho người trưởng thành và thanh thiếu niên chưa từng nhiễm virus SARS-CoV-2 cũng như không tiếp xúc với ca mắc COVID-19 nào trong thời gian gần đây. Tuy nhiên, việc phòng bệnh dựa trên hỗn hợp kháng thể Evusheld không thay thế cho việc tiêm phòng ở những đối tượng đủ điều kiện tiêm vaccine ngừa COVID-19. Theo các kết quả thử nghiệm giai đoạn cuối được công bố vào tháng 8 năm nay, Evusheld giúp giảm 77% nguy cơ triệu chứng bệnh trở nặng ở người mắc COVID-19.Trong khi vaccine dựa vào hệ thống miễn dịch nguyên vẹn để phát triển các kháng thể "nhắm trúng mục tiêu" và các tế bào chống nhiễm trùng, thì hỗn hợp kháng thể Evusheld chứa các kháng thể được tạo ra trong phòng thí nghiệm sẽ giúp các kháng thể này tồn tại trong cơ thể nhiều tháng từ đó có thể chống lại virus SARS-CoV-2 khi người tiêm Evusheld mắc COVID-19.
Người sử dụng liệu pháp này sẽ được tiêm 2 mũi liên tiếp và cocktail kháng thể có thể có tác dụng kéo dài từ vài tháng cho đến một năm.
Bà Patrizia Cavazzoni, Giám đốc Trung tâm Nghiên cứu và Đánh giá thuốc của FDA, nhấn mạnh mặc dù các loại vaccine hiện cung cấp khả năng phòng ngừa tốt nhất với COVID-19 nhưng một số cá nhân có hệ miễn dịch bị tổn thương hoặc những người có tiền sử bị tác dụng phụ với vaccine cần có một lựa chọn thay thế. Quyết định mới nhất này đối với liệu pháp cocktail kháng thể - được tạo thành từ hai loại kháng thể đơn dòng tixagevimab và cilgavimab - đánh dấu một bước tiến quan trọng đối với AstraZeneca trong bối cảnh vaccine ngừa COVID-19 của công ty dược phẩm đa quốc gia tại Anh và Thụy Điển này vẫn chưa được các cơ quan có thẩm quyền của Mỹ cấp phép sử dụng tại nước này. Tháng trước, AstraZeneca đã nhất trí cung cấp cho Mỹ 700.000 liều Evusheld./.Tin liên quan
-
![Tìm ra nguyên nhân của biến chứng đông máu sau tiêm vaccine AstraZeneca]() Kinh tế xã hội
Kinh tế xã hội
Tìm ra nguyên nhân của biến chứng đông máu sau tiêm vaccine AstraZeneca
20:30' - 02/12/2021
Các nhà khoa học Anh và Mỹ mới đây đã tìm ra nguyên nhân dẫn đến tình trạng đông máu hiếm gặp sau khi tiêm vaccine ngừa COVID-19 do AstraZeneca sản xuất.
-
![Thuốc kháng thể chống COVID-19 của Astrazeneca có hiệu quả bảo vệ trong 6 tháng]() Kinh tế xã hội
Kinh tế xã hội
Thuốc kháng thể chống COVID-19 của Astrazeneca có hiệu quả bảo vệ trong 6 tháng
16:32' - 18/11/2021
Ngày 18/11, hãng dược phẩm AstraZeneca (Anh-Thụy Điển) cho biết thuốc kháng thể chống COVID-19 dạng tiêm mang tên Evusheld của hãng này cho hiệu quả bảo vệ lên đến 83% trong vòng 6 tháng.
Tin cùng chuyên mục
-
![XSMB 11/5. Kết quả xổ số miền Bắc hôm nay ngày 11/5/2026. XSMB thứ Hai ngày 11/5]() Kinh tế xã hội
Kinh tế xã hội
XSMB 11/5. Kết quả xổ số miền Bắc hôm nay ngày 11/5/2026. XSMB thứ Hai ngày 11/5
19:30'
Bnews. XSMB 11/5. Kết quả xổ số hôm nay ngày 11/5. XSMB thứ Hai. Trực tiếp KQXSMB ngày 11/5. Kết quả xổ số miền Bắc hôm nay thứ Hai ngày 11/5/2026
-
![XSMN 11/5. Kết quả xổ số miền Nam hôm nay ngày 11/5/2026. XSMN thứ Hai ngày 11/5]() Kinh tế xã hội
Kinh tế xã hội
XSMN 11/5. Kết quả xổ số miền Nam hôm nay ngày 11/5/2026. XSMN thứ Hai ngày 11/5
19:30'
XSMN 11/5. KQXSMN 11/5/2026. Kết quả xổ số hôm nay ngày 11/5. XSMN thứ Hai. Xổ số miền Nam hôm nay 11/5/2026. Trực tiếp KQXSMN ngày 11/5. Kết quả xổ số miền Nam hôm nay thứ Hai ngày 11/5/2026.
-
![XSMT 11/5. Kết quả xổ số miền Trung hôm nay ngày 11/5/2026. XSMT thứ Hai ngày 11/5]() Kinh tế xã hội
Kinh tế xã hội
XSMT 11/5. Kết quả xổ số miền Trung hôm nay ngày 11/5/2026. XSMT thứ Hai ngày 11/5
19:30'
Bnews. XSMT 11/5. Kết quả xổ số hôm nay ngày 11/5. XSMT thứ Hai. Trực tiếp KQXSMT ngày 11/5. Kết quả xổ số miền Trung hôm nay thứ Hai ngày 11/5/2026.
-
![Virus Hanta: Hành khách bắt đầu rời tàu MV Hondius]() Kinh tế xã hội
Kinh tế xã hội
Virus Hanta: Hành khách bắt đầu rời tàu MV Hondius
19:29'
Ngày 10/5, giới chức Tây Ban Nha xác nhận hành khách trên tàu du lịch MV Hondius treo cờ Hà Lan đã bắt đầu rời tàu, vài giờ sau khi tàu cập bến Tenerife, thuộc quần đảo Canary của Tây Ban Nha.
-
![XSĐT 11/5. Kết quả xổ số Đồng Tháp hôm nay ngày 11/5/2026. SXĐT ngày 11/5]() Kinh tế xã hội
Kinh tế xã hội
XSĐT 11/5. Kết quả xổ số Đồng Tháp hôm nay ngày 11/5/2026. SXĐT ngày 11/5
19:00'
Bnews. XSĐT 11/5. Kết quả xổ số hôm nay ngày 11/5. XSĐT Thứ Hai. Trực tiếp KQXSĐT ngày 11/5. Kết quả xổ số Đồng Tháp hôm nay ngày 11/5/2026. Kết quả xổ số Đồng Tháp Thứ Hai ngày 11/5/2026.
-
![Kết quả xổ số Hồ Chí Minh hôm nay ngày 11/5/2026. XSHCM ngày 11/5. XSHCM 11/5]() Kinh tế xã hội
Kinh tế xã hội
Kết quả xổ số Hồ Chí Minh hôm nay ngày 11/5/2026. XSHCM ngày 11/5. XSHCM 11/5
19:00'
Bnews. XSHCM 11/5. Kết quả xổ số hôm nay ngày 11/5. XSHCM Thứ Hai. Trực tiếp KQXSHCM. Kết quả xổ số Hồ Chí Minh hôm nay ngày 11/5/2026.Kết quả xổ số Hồ Chí Minh ngày 11/5/2026. XS Sài Gòn.
-
![Kết quả xổ số Cà Mau hôm nay ngày 11/5/2026. SXCM ngày 11/5. XSCM 11/5]() Kinh tế xã hội
Kinh tế xã hội
Kết quả xổ số Cà Mau hôm nay ngày 11/5/2026. SXCM ngày 11/5. XSCM 11/5
19:00'
Bnews. XSCM. Kết quả xổ số hôm nay ngày 11/5. XSCM Thứ Hai. Trực tiếp KQXSCM ngày 11/5. Kết quả xổ số Cà Mau hôm nay ngày 11/5/2026. Kết quả xổ số Cà Mau Thứ Hai ngày 11/5/2026.
-
![XSPY 11/5. Kết quả xổ số Phú Yên hôm nay ngày 11/5/2026. XSPY ngày 11/5. XSPY 11/5]() Kinh tế xã hội
Kinh tế xã hội
XSPY 11/5. Kết quả xổ số Phú Yên hôm nay ngày 11/5/2026. XSPY ngày 11/5. XSPY 11/5
18:00'
XSPY 11/5. Kết quả xổ số Phú Yên hôm nay ngày 11/5/2026. XSPY ngày 11/5. XSPY 11/5. Kết quả xổ số Phú Yên hôm nay ngày 11/5/2026. XSPY ngày 11/5. XSPY hôm nay
-
![XSTTH 11/5. Kết quả xổ số Thừa Thiên Huế hôm nay ngày 11/5/2026. XSTTH ngày 11/5. XSTTH hôm nay]() Kinh tế xã hội
Kinh tế xã hội
XSTTH 11/5. Kết quả xổ số Thừa Thiên Huế hôm nay ngày 11/5/2026. XSTTH ngày 11/5. XSTTH hôm nay
18:00'
XSTTH 11/5. Kết quả xổ số hôm nay ngày 11/5. XSTTH Thứ Hai. Trực tiếp KQXSTTH ngày 11/5. Kết quả xổ số Thừa Thiên Huế hôm nay ngày 11/5/2026.

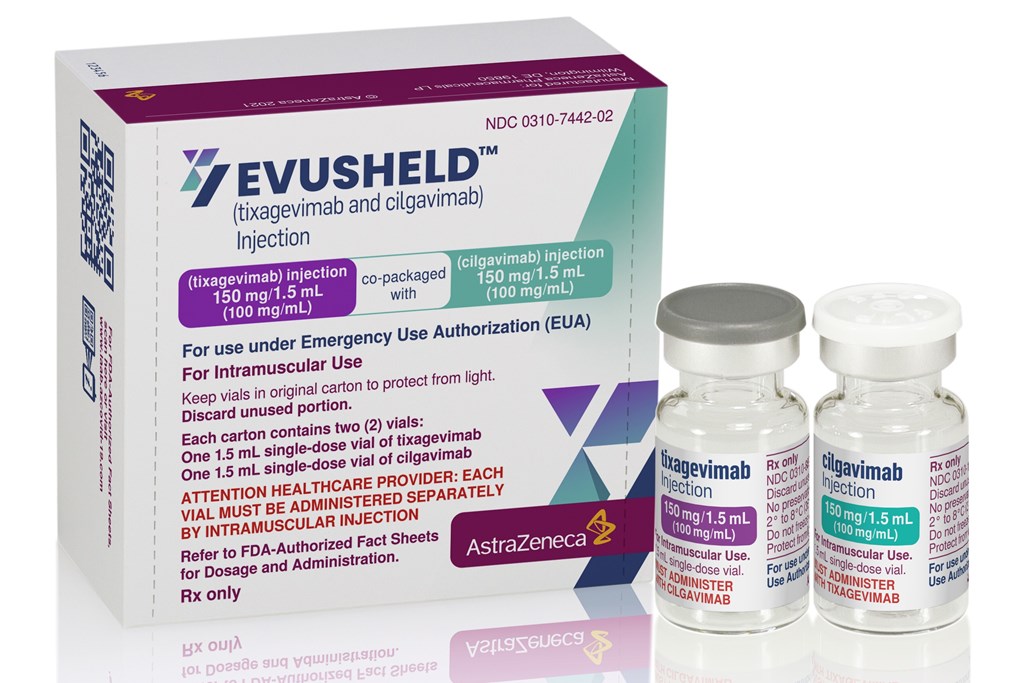 Cocktail kháng thể Evusheld phòng COVID-19 của AstraZeneca. Ảnh: Reuters
Cocktail kháng thể Evusheld phòng COVID-19 của AstraZeneca. Ảnh: Reuters