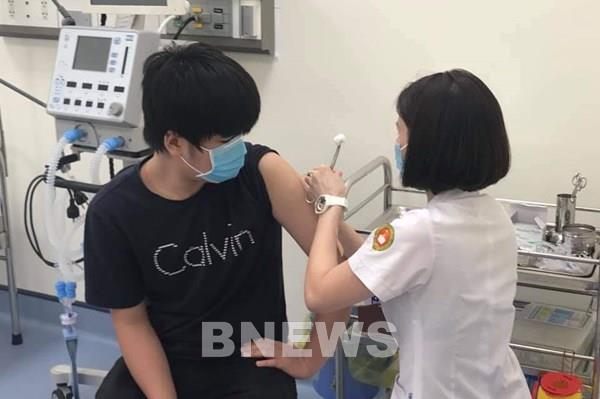
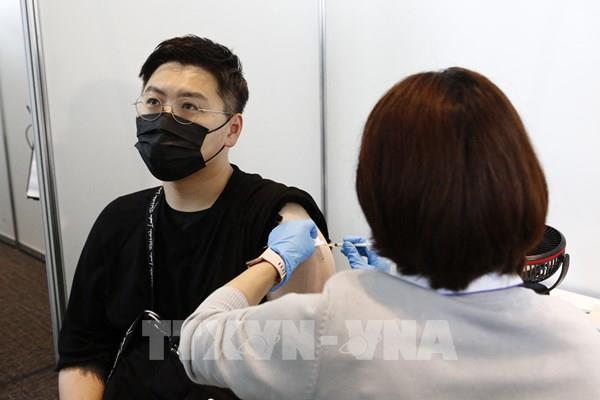
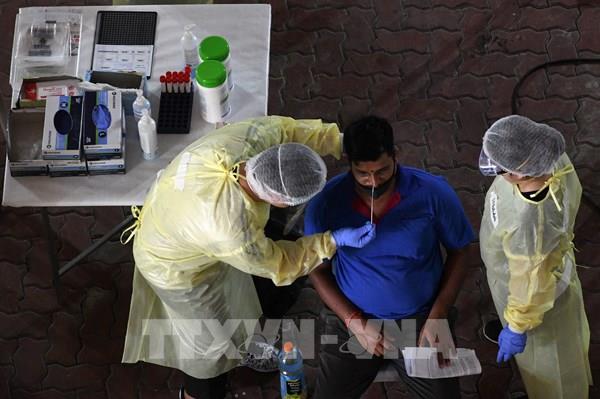
Vaccine Nanocovax: Nanogen phải bổ sung hồ sơ về những nội dung gì?
Ngày 29/8, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, Bộ Y tế đã họp và đề nghị tiếp tục bổ sung hồ sơ vaccine COVID-19 Nanocovax.
Theo đó, Hội đồng tư vấn ghi nhận các kết quả đạt được đối với hồ sơ đề nghị cấp Giấy đăng ký lưu hành của vaccine Nanocovax đã được các tiểu ban chuyên môn thẩm định, Hội đồng Đạo đức nghiệm thu. Đồng thời, Hội đồng tư vấn đề nghị doanh nghiệp tiếp tục bổ sung, làm rõ một số nội dung.Cụ thể, về hồ sơ chất lượng, căn cứ kết quả thẩm định của tiểu ban chất lượng, đề nghị doanh nghiệp bổ sung, cập nhật một số nội dung theo ý kiến của tiểu ban chất lượng theo hình thức cuốn chiếu.Về hồ sơ dược lý, lâm sàng, căn cứ kết quả thẩm định hồ sơ lâm sàng của Trung tâm Dược lý lâm sàng - Trường Đại học Y Hà Nội và Kết luận của Hội đồng Đạo đức tại Biên bản số 56/BB-HĐĐĐ ngày 22/8/2021, Hội đồng tư vấn đề nghị, doanh nghiệp cần bổ sung, cập nhật thêm dữ liệu an toàn cho toàn bộ đối tượng đã được tiêm ít nhất một liều vaccine tới thời điểm hiện tại và giải thích rõ về các trường hợp sự cố bất lợi nghiêm trọng (SAE) tới thời điểm hiện tại.Về tính sinh miễn dịch, doanh nghiệp bổ sung, cập nhật dữ liệu theo Đề cương sửa đổi mới nhất được Hội đồng đạo đức thông qua, bao gồm: Bổ sung, cập nhật đánh giá tính sinh miễn dịch trên các biến chủng mới (ví dụ biến chủng Delta, biến chủng Anh…) và cỡ mẫu đánh giá tính sinh miễn dịch cần thực hiện theo đúng đề cương nghiên cứu đã được thông qua.Về hiệu quả bảo vệ, doanh nghiệp phối hợp với nhóm nghiên cứu để phân tích, bàn luận về mối liên quan giữa tính sinh miễn dịch của vaccine và hiệu quả bảo vệ tối thiểu 50% (theo hướng dẫn của Tổ chức Y tế thế giới - WHO) dựa trên các dữ liệu y văn.Hội đồng cũng đề nghị doanh nghiệp khẩn trương bổ sung, cập nhật các nội dung nêu trên, báo cáo Hội đồng Đạo đức và Hội đồng tư vấn tiếp tục xem xét, thẩm định cuốn chiếu các kết quả nghiên cứu để có thể cấp giấy đăng ký lưu hành có điều kiện trong trường hợp cấp bách.Nanocovax là vaccine COVID-19 do Công ty Cổ phần công nghệ sinh học Dược Nanogen nghiên cứu, phát triển, một liệu trình hai liều tiêm cách nhau 28 ngày. Để thúc đẩy tiến độ thử nghiệm lâm sàng vaccine trong bối cảnh đại dịch, Bộ Y tế đã cho phép sử dụng các kết quả giữa kỳ của nghiên cứu thử nghiệm lâm sàng để đánh giá, sau đó gối vụ thử nghiệm.
Thông tin từ Bộ Y tế cho biết, đến thời điểm này, ứng viên vaccine Nanocovax đang thử nghiệm lâm sàng giai đoạn 2 của pha 3 và đã hoàn thành tiêm 2 mũi vaccine cho 13.000 người tình nguyện của giai đoạn 3, dự kiến đến ngày 10/9/2021 sẽ hoàn thành các xét nghiệm đánh giá tính sinh miễn dịch sau 42 ngày tiêm vaccine mũi 1 của giai đoạn 3a. Từ góc độ của Bộ Y tế - cơ quan quản lý nhà nước, tại một số cuộc họp về nghiên cứu, sản xuất vaccine trong nước, Thứ trưởng Trần Văn Thuấn nhấn mạnh việc cấp phép cần dựa trên những bằng chứng khách quan, minh bạch, khoa học được Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia và Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc xem xét, đánh giá.Đây là hai Hội đồng độc lập và Bộ Y tế sẽ xem xét việc cấp phép đối với một thuốc, vaccine khi thuốc, vaccine đó được hai Hội đồng thông qua.Vaccine là sản phẩm đặc biệt, không chỉ có tác động tới một người mà cả cộng đồng, chính vì vậy cần xem xét cẩn thận, kỹ lưỡng, đặc biệt có sự tham vấn của các nhà khoa học uy tín, các tổ chức quốc tế như Tổ chức Y tế Thế giới (WHO), Trung tâm kiểm soát và phòng ngừa dịch bệnh Hoa Kỳ (USCDC)… và có những bước đi cẩn trọng từng bước để có thể đánh giá về tính an toàn (ngắn hạn và dài hạn), sự ổn định và sự bền vững của tính sinh miễn dịch, đặc biệt là hiệu quả bảo vệ./.>>Để cấp phép khẩn cấp vaccine cần đáp ứng điều kiện gì?
Tin liên quan
-
![Việt Nam tiếp nhận thêm hơn 250.000 liều vaccine phòng COVID-19]() Kinh tế xã hội
Kinh tế xã hội
Việt Nam tiếp nhận thêm hơn 250.000 liều vaccine phòng COVID-19
15:36' - 30/08/2021
Ngày 30/8, tại Bộ Y tế đã diễn ra lễ trao tặng 250.800 liều vaccine phòng COVID-19 AstraZeneca và Moderna do Chính phủ Cộng hoà Séc tài trợ cho Việt Nam.
-
![Đề nghị Nanogen tiếp tục bổ sung hồ sơ cho vaccine NANOCOVAX]() Kinh tế Việt Nam
Kinh tế Việt Nam
Đề nghị Nanogen tiếp tục bổ sung hồ sơ cho vaccine NANOCOVAX
21:04' - 29/08/2021
Hội đồng tư vấn ghi nhận các kết quả đạt được đối với hồ sơ đề nghị cấp Giấy đăng ký lưu hành của vaccine Nanocovax đã được các tiểu ban chuyên môn thẩm định, Hội đồng Đạo đức nghiệm thu.
-
![Nhật Bản cân nhắc cho phép tiêm kết hợp các vaccine khác nhau]() Kinh tế Thế giới
Kinh tế Thế giới
Nhật Bản cân nhắc cho phép tiêm kết hợp các vaccine khác nhau
17:16' - 29/08/2021
Bộ Y tế Nhật Bản đang cân nhắc khả năng tiêm kết hợp các loại vaccine ngừa COVID-19 khác nhau nhằm giảm bớt quan ngại về nguồn cung và đẩy nhanh chương trình tiêm chủng tại quốc gia này.
-
![Tỷ lệ bao phủ vaccine ngừa COVID-19 của Singapore cao nhất thế giới]() Kinh tế xã hội
Kinh tế xã hội
Tỷ lệ bao phủ vaccine ngừa COVID-19 của Singapore cao nhất thế giới
12:52' - 29/08/2021
Singapore đã trở thành nước có tỷ lệ tiêm chủng vaccine phòng COVID-19 cao nhất thế giới với 80% dân số nước này đã được tiêm đầy đủ.
Tin cùng chuyên mục
-
![Những điểm mới của Giải thưởng Thiếu nhi Dế Mèn 2026]() Kinh tế xã hội
Kinh tế xã hội
Những điểm mới của Giải thưởng Thiếu nhi Dế Mèn 2026
23:37' - 22/05/2026
Giải thưởng năm nay được trao cho những sáng tác, trình diễn nghệ thuật xuất sắc “của thiếu nhi” và “vì thiếu nhi”.
-
![Kết quả giải thưởng Dế mèn 2026]() Kinh tế xã hội
Kinh tế xã hội
Kết quả giải thưởng Dế mèn 2026
23:20' - 22/05/2026
Kết quả mùa giải năm nay đã cho thấy biên độ sáng tạo ngày càng được mở rộng ở cả khía cạnh tác giả lẫn tác phẩm.
-
![Triển lãm “Thế giới tuổi thơ qua các tác phẩm của cố NSND Ngô Mạnh Lân”]() Kinh tế xã hội
Kinh tế xã hội
Triển lãm “Thế giới tuổi thơ qua các tác phẩm của cố NSND Ngô Mạnh Lân”
22:50' - 22/05/2026
Từ ngày 22 đến 24/5/2026, tại Bảo tàng Mỹ thuật Việt Nam diễn ra triển lãm “Thế giới tuổi thơ qua các tác phẩm của cố NSND Ngô Mạnh Lân”.
-
![Chuyên gia khuyến cáo “5 không” để bảo vệ dữ liệu cá nhân]() Kinh tế xã hội
Kinh tế xã hội
Chuyên gia khuyến cáo “5 không” để bảo vệ dữ liệu cá nhân
20:35' - 22/05/2026
Các chuyên gia an ninh mạng cảnh báo tình trạng mua bán dữ liệu cá nhân ngày càng phức tạp, đòi hỏi doanh nghiệp và người dùng nâng cao năng lực bảo vệ dữ liệu trong môi trường số.
-
![XSMB 23/5. Kết quả xổ số miền Bắc hôm nay ngày 23/5/2026. XSMB thứ Bảy ngày 23/5]() Kinh tế xã hội
Kinh tế xã hội
XSMB 23/5. Kết quả xổ số miền Bắc hôm nay ngày 23/5/2026. XSMB thứ Bảy ngày 23/5
20:04' - 22/05/2026
Bnews. XSMB 23/5. Kết quả xổ số hôm nay ngày 23/5. XSMB thứ Bảy. Trực tiếp KQXSMB ngày 23/5. Kết quả xổ số miền Bắc hôm nay thứ Bảy ngày 23/5/2026.
-
![XSMN 23/5. Kết quả xổ số miền Nam hôm nay ngày 23/5/2026. XSMN thứ Bảy ngày 23/5]() Kinh tế xã hội
Kinh tế xã hội
XSMN 23/5. Kết quả xổ số miền Nam hôm nay ngày 23/5/2026. XSMN thứ Bảy ngày 23/5
19:30' - 22/05/2026
XSMN 23/5. KQXSMN 23/5/2026. Kết quả xổ số hôm nay ngày 23/5. XSMN thứ Bảy. Xổ số miền Nam hôm nay 23/5/2026. Trực tiếp KQXSMN ngày 23/5. Kết quả xổ số miền Nam hôm nay thứ Bảy ngày 23/5/2026.
-
![XSMT 23/5. Kết quả xổ số miền Trung hôm nay ngày 23/5/2026. XSMB thứ Bảy ngày 23/5]() Kinh tế xã hội
Kinh tế xã hội
XSMT 23/5. Kết quả xổ số miền Trung hôm nay ngày 23/5/2026. XSMB thứ Bảy ngày 23/5
19:30' - 22/05/2026
Bnews. XSMT 23/5. Kết quả xổ số hôm nay ngày 23/5. XSMT thứ Bảy. Trực tiếp KQXSMT ngày 23/5. Kết quả xổ số miền Trung hôm nay thứ Bảy ngày 23/5/2026.
-
![Kết quả Vietlott Power 6/55 ngày 23/5 - Kết quả xổ số Vietlott ngày 23/5/2026 - Xổ số Vietlott Power 6/55 hôm nay]() Kinh tế xã hội
Kinh tế xã hội
Kết quả Vietlott Power 6/55 ngày 23/5 - Kết quả xổ số Vietlott ngày 23/5/2026 - Xổ số Vietlott Power 6/55 hôm nay
19:30' - 22/05/2026
Bnews. Kết quả Vietlott Power 6/55 ngày 23/5. Kết quả xổ số Vietlott hôm nay ngày 23 tháng 5 năm 2026 - Xổ số Vietlott Power 6/55 hôm nay.
-
![XSBP 23/5. Kết quả xổ số Bình Phước hôm nay ngày 23/5/2026. SXBP ngày 23/5]() Kinh tế xã hội
Kinh tế xã hội
XSBP 23/5. Kết quả xổ số Bình Phước hôm nay ngày 23/5/2026. SXBP ngày 23/5
19:00' - 22/05/2026
Bnews. XSBP 23/5. Kết quả xổ số hôm nay ngày 23/5. XSBP Thứ Bảy. Trực tiếp KQXSBP ngày 23/5. Kết quả xổ số Bình Phước hôm nay ngày 23/5/2026.

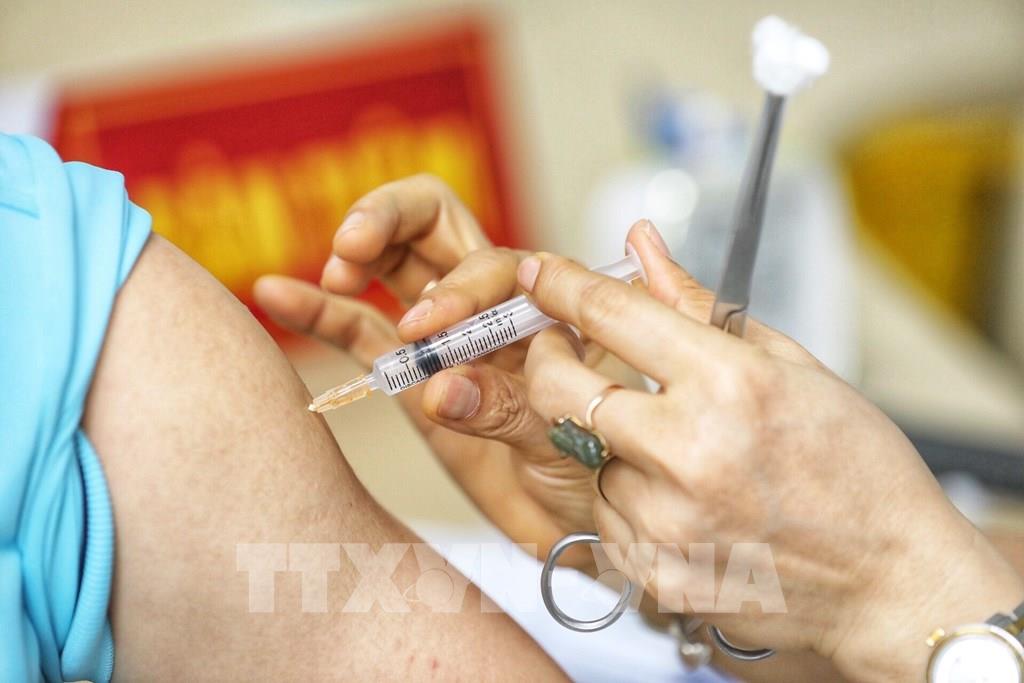 Nhân viên y tế tiêm thử nghiệm vaccine Nano Covax phòng COVID-19 giai đoạn 3. Ảnh: Minh Quyết - TTXVN
Nhân viên y tế tiêm thử nghiệm vaccine Nano Covax phòng COVID-19 giai đoạn 3. Ảnh: Minh Quyết - TTXVN  Nhân viên y tế tiêm thử nghiệm vaccine Nano Covax phòng COVID-19 giai đoạn 3. Ảnh: Minh Quyết - TTXVN
Nhân viên y tế tiêm thử nghiệm vaccine Nano Covax phòng COVID-19 giai đoạn 3. Ảnh: Minh Quyết - TTXVN